Nature оцінює витрати великих фармацевтичних компаній на відкриття, клінічні випробування і патентування одного лікарського засобу в $0,5–2,6 млрд і 10–20 років досліджень. Більша частина цих грошей, по суті, викидається на вітер — лише кілька з десятків, а то й сотень тестових молекул знаходять своє застосування в нових препаратах. Тому фармацевтичні гіганти й сотні стартапів вкладаються в розробку комп’ютерних алгоритмів, які були б здатні пришвидшити та здешевити цей процес.
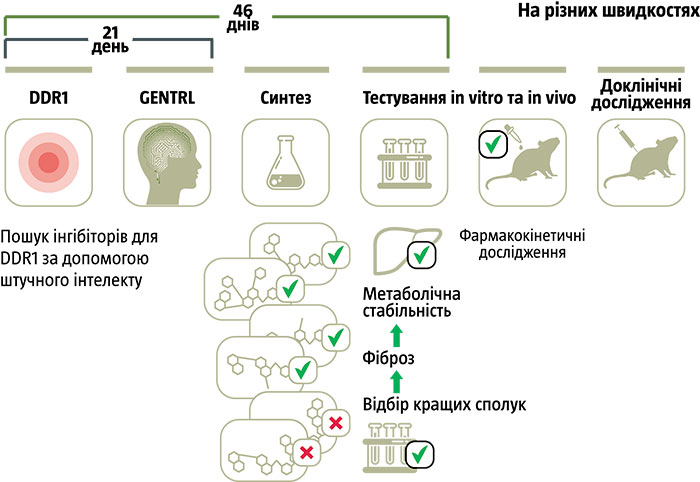
Компанія Insilico Medicine, що базується в Балтіморі та Гонконзі, може стати революціонером у галузі комп’ютерного передбачення структури лікарських молекул: її алгоритм GENTRL лише за 21 день знайшов інгібітор для білка DDR1 (див. «На різних швидкостях»), пов’язаного з виникненням фіброзу. Дискодиновий доменний рецептор DDR1 залучений до процесів клітинного росту, клітинної диференціації та метаболізму. Він міститься в клітинах епітелію і, як вважається, відіграє вагому роль у появі фіброзу — ущільнення сполучної тканини, що виникає задля ізоляції джерела запалення від інших органів та кровотоку. Наприклад, при фіброзі легенів, який може бути спричинений запаленням, бронхи та легені збільшуються в розмірі, навколо кровоносних і лімфатичних судин утворюється щільна сполучна тканина. Пригнічення роботи DDR1 вважається потенційним способом запобігання фіброзу та його лікування.
Читайте також: Штучний інтелект: загроза чи незріла технологія
Нейронна мережа як вхідні дані використовувала відкриту базу ZINC, що складається з 230 млн хімічних сполук, придатних для комерційного використання, а також базу відомих інгібіторів DDR1, звичайних інгібіторів кінази, фармацевтичну базу даних відомих біологічно активних молекул. Програма згенерувала 30 тис. молекул, які автоматично перевірила на наявність у базі запатентованих речовин серед усіх відомих інгібіторів кінази і специфічно серед інгібіторів DDR1. Залишилося шість молекул, із яких одна дійшла до випробування на мишах.
«Кінази — це тип ферментів, що фосфорелюють білки, тобто переносять на них фосфатні групи. У клітині вони працюють фактично як молекулярні перемикачі для прийому зовнішньоклітинних сигналів і передачі їх далі аж до ядра та активації певних генів. В одному сигнальному шляху можуть бути задіяні десятки кіназ: одна фосфорелює одну ціль, інша — наступну і так далі. Білок DDR1 — це тирозинова кіназа, тобто вона фосфорелює амінокислоту тирозин, а ще це зовнішньоклітинний рецептор колагену, «вимкнення» якого — перспективна модель боротьби з фіброзом. Активація DDR1 спричиняє запалення, що безпосередньо пов’язане з розвитком фіброзу. Завдання авторів дослідження — зупинити дію DDR1, щоб він не фосфорелював. І зробити це cелективно, тобто не зачепивши будь-які інші білки, що з дуже великою ймовірністю буде небезпечним», — пояснює Федір Боховчук, Ph.D із біохімії і науковий співробітник однієї з великих фармкомпаній.
Згідно з дослідженням Insilico Medicine знайдена молекула має діяти саме на білок DDR1, не зачіпаючи інших сполук. Це важливий результат, що зменшує ймовірність токсичної дії на інші системи організму.
«Штучний інтелект може швидко перевірити взаємодію нової молекули з усіма можливими білковими структурами, просканувати, чи не діє вона на інші цілі, не передбачені для того. Це важко зробити експериментально. Адже кількість мішеней, що є на лабораторному столі дослідників, завжди обмежена. І не можна бути певним, що експериментатори перебрали всі можливі варіанти. Тоді як програма здатна перебрати навіть нещодавно відкриті сполуки або білки з організмів риб чи мишей, експериментальних даних щодо яких наразі небагато. І віднайти можливу токсичну дію, аналізуючи взаємодію зі схожим білком уже в людини. Складність цього завдання пов’язана також із нашим неповним розумінням біології, обмеженим розумінням ролі кожного гена та білка. Якщо активується ген А, що буде з геном B? Як мутація в гені А відгукнеться на рівні експресії інших генів? На сьогодні є велетенські масиви генетичних та епігенетичних даних, отриманих за допомогою секвенування ДНК і РНК тисяч людей. Штучний інтелект видається перспективним інструментом для того, щоб виявити всі ці взаємодії», — коментує Федір Боховчук.
Проблеми, що виникають через брак знань у царині взаємодії ліків із різними системами організму, можна проілюструвати скандалом із тербінафіном. У 1996 році австралійські медики відзначили, що популярні ліки від грибкових інфекцій призводять до запалення печінки. Після трьох смертей, спричинених вживанням тербінафіну, препарати стали перевіряти. У 2001-му канадські науковці знайшли в печінці постраждалих людей сполуку TBF-A, що могла мати токсичну дію. Лише у 2018-му загадку тербінафіну розгадали — за допомогою нейронних мереж. Дослідники просканували всі можливі шляхи метаболізму тербінафіну в печінці й зрозуміли, яким чином ліки перетворюються на токсичну TBF-A. Метаболітичний процес складався з двох кроків, і передбачити подібне під час клінічних випробовувань лікарі не могли. Натомість із цим завданням впорався штучний інтелект.
Читайте також: Як штучний інтелект піклується про здоров’я людей
Компанію Insilico Medicine заснував у 2014 році біоінформатик Алєксандр Жаворонков, він же головний автор нещодавнього дослідження. За п’ять років вона залучила понад $50 млн інвестицій, переважно на дослідження процесів старіння методами штучного інтелекту. Зокрема, у січні 2019-го була опублікована стаття про вплив куріння на старіння організму. За біохімічним складом крові було встановлено, що за деякими показниками, як-от рівень холестеролу та рівень глюкози, курці приблизно вдвічі старіші за свій біологічний вік. У 2016-му компанія представила програму GeroScope для пошуку геропротекторів — «ліків від старіння». Логіка в тому, щоб порівняти стан клітин людей від 15 до 30 років із клітинами людей, яким за 60, і знайти молекулярні шлях перетворення молодих клітин на старі. Щоправда, наразі жоден із геропротекторів, які дають результати на тваринах, не дозволений для використання людьми.
Біоінформатик із Кембриджського університету доктор Андреас Бендер у своєму блозі, присвяченому пошуку хімічних сполук за допомогою штучного інтелекту, закликає ставитися до дослідження Insilico Medicine з обережністю. За його словами, нова молекула на 75% збігається з уже відомими інгібіторами DDR1, тому вона не є «абсолютно новою». До того ж більшість потенційних ліків провалюють клінічні дослідження, тому казати, що штучний інтелект створив нові ліки, некоректно. Бендер висловлює сумнів, що програма Insilico Medicine спрацювала б так само добре без бази відомих інгібіторів кінази для відкриття справді нової молекули, проте зазначив, що дослідження компанії все ж таки є важливим етапом становлення штучного інтелекту в пошуку нових лікарських сполук.

